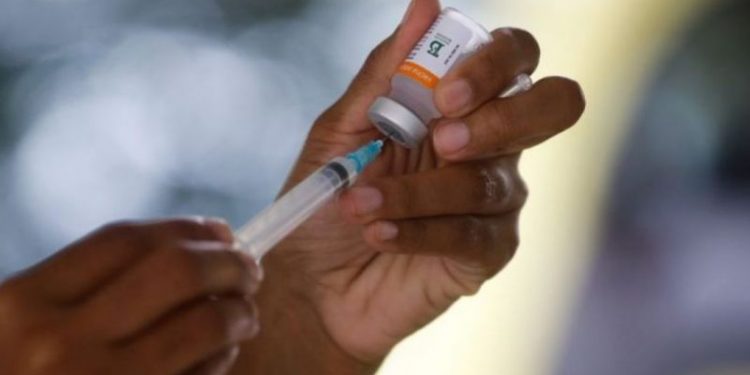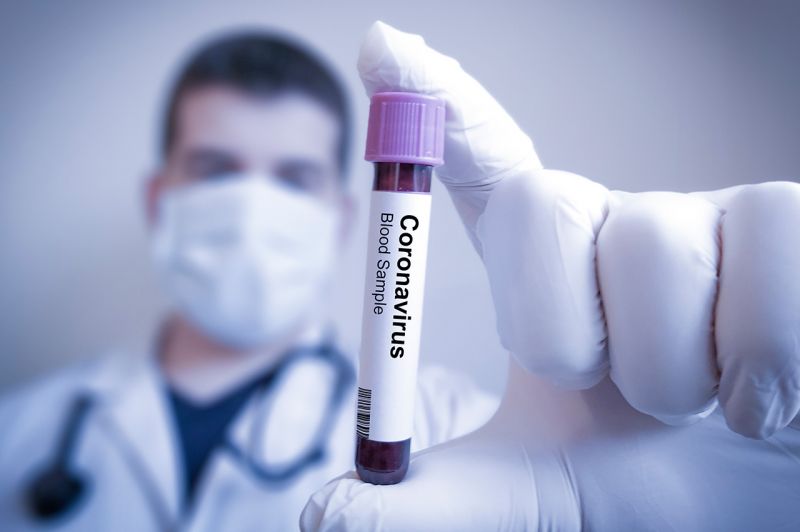
A Agência Nacional de Vigilância Sanitária (Anvisa) liberou a prática de pesquisas clínicas referentes à duas novas vacinas contra o coronavírus. A autorização aconteceu nesta quarta-feira, 14 de julho.
Uma delas é produzida pelo Instituto de Biologia Médica da Academia Chinesa de Ciências Médicas (Imbcams, na sigla em inglês), da China, enquanto a outra é de responsabilidade da empresa AstraZeneca.
Essa pesquisa, que deve ser realizada em solo brasileiro, é apenas uma parte de um grande estudo que já está sendo pauta em outros países.
Ainda na fase de testes, adultos de 18 anos ou mais deverão receber duas doses dessas vacinas, com intervalo de 14 dias entre uma dose e outra.
De acordo com a Anvisa, “o delineamento de um estudo controlado por placebo ainda é considerado metodologicamente adequado para avaliar a segurança e eficácia da vacina, considerando também que ainda há uma grande parcela da população não vacinada, desde que se leve em conta a possibilidade de acesso dos voluntários às vacinas disponíveis em um curto período”.
Mais de 34 mil pessoas participarão dos testes no Brasil, Malásia, Bangladesh, China e México. Desse total, 7.992 são brasileiros. Santa Catarina está entre os estados selecionados para participar desse estudo, juntamente com Rio de Janeiro, Goiás e São Paulo.